In de afgelopen 40 jaar hebben talrijke studies de mogelijke link tussen extreem lagefrequente elektrische en magnetische velden (ELF-EMV) en gezondheid onderzocht. Korte termijn – hoge intensiteit blootstelling werd grondig bestudeerd bij menselijke vrijwilligers en bij dieren. De waargenomen effecten komen niet voor onder bepaalde drempelwaarden en kunnen worden vermeden door te voldoen aan geschikte basisbeperkingen voor de in het lichaam geïnduceerde elektrische velden.
Er rijzen vragen over lange termijn – lage intensiteit blootstelling. ELF-MV worden door IARC geclassificeerd als “mogelijk carcinogeen voor de mens” op basis van epidemiologisch bewijs dat duidt op een verhoogd risico op leukemie bij kinderen. Andere studies richten zich op de mogelijke rol van 50 Hz EMV bij de ontwikkeling van kanker, de ziekte van Alzheimer en andere ziektes. De studies zijn echter niet doorslaggevend en verder onderzoek is nodig.
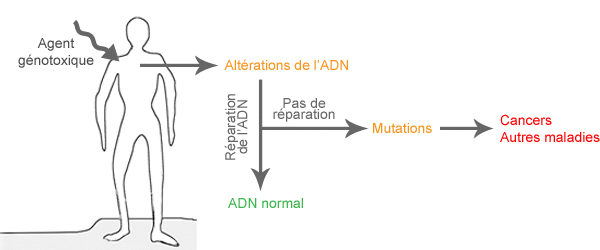
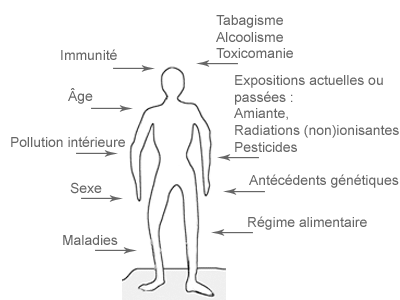
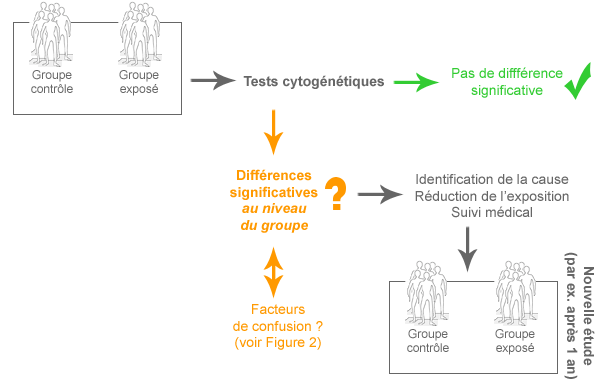
Daarom is het belangrijk om de biologische gevolgen te bepalen bij typisch blootgestelde groepen, zoals aan EMV blootgestelde werknemers. Een cytogenetisch biomonitoringonderzoek is nuttig om na te gaan of ELF-EMV al dan niet genetische schade kan veroorzaken.
Wat is een cytogenetische biomonitoringstudie en hoe zou dit kunnen helpen bij het begrijpen van de gezondheidseffecten van elektromagnetische velden? Het hier volgende overzicht geeft weer hoe een cytogenetisch monitoringonderzoek wordt uitgevoerd en hoe het moet worden geïnterpreteerd.